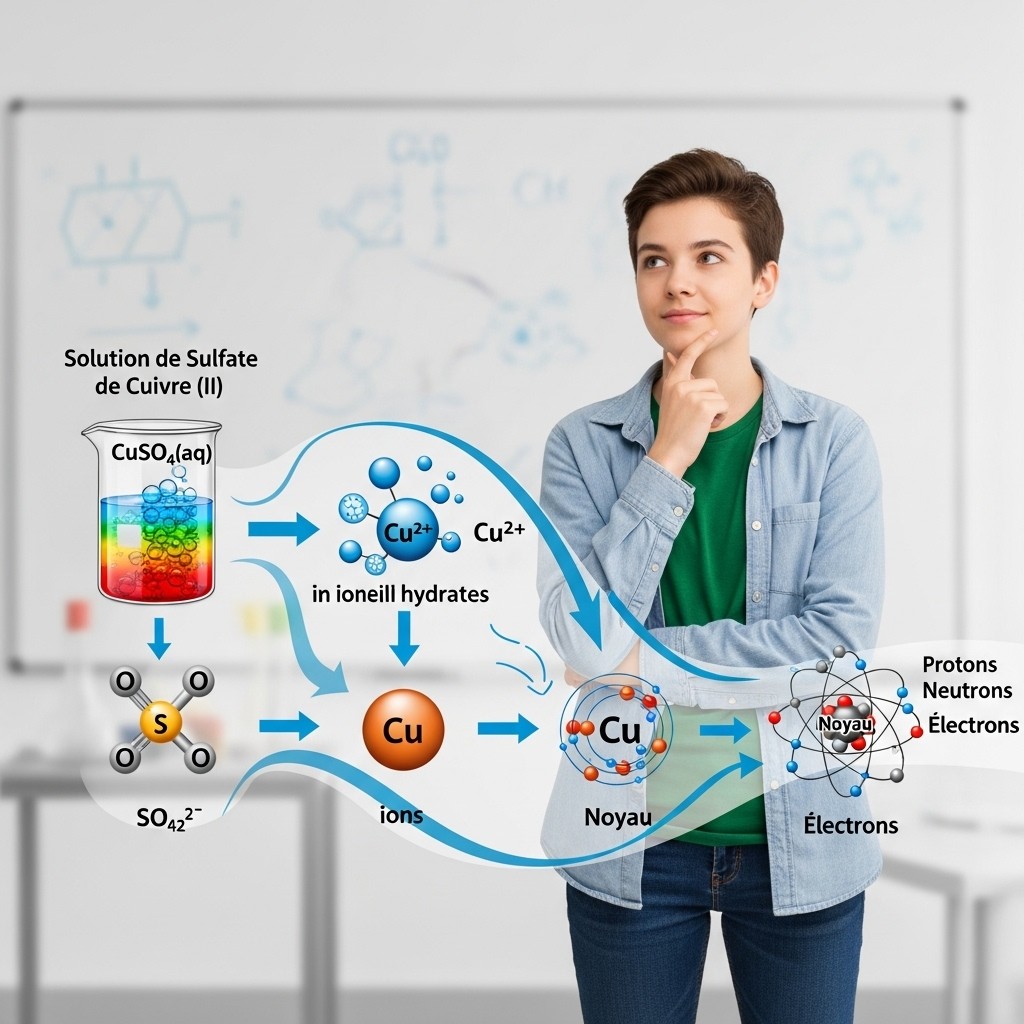
FICHE DE RÉVISION – De l'espèce chimique à l'entité atomique
(Niveau : Seconde)
Matière : De l’Espèce Chimique à l’Entité Atomique
Plonger au cœur de la matière : atomes, ions, molécules, structure du noyau et configuration électronique.
Partie 1 : Espèces et Entités Chimiques
On distingue la description de la matière à grande échelle (macroscopique) et à très petite échelle (microscopique).
1. Espèce Chimique (Macroscopique) vs Entité Chimique (Microscopique)
Une espèce chimique est une collection d’un très grand nombre (des milliards de milliards…) d’entités chimiques identiques.
Les entités chimiques sont les constituants microscopiques de la matière. Il en existe trois types principaux :
- Atome : La « brique » de base neutre électriquement (ex : atome de fer Fe, atome d’oxygène O).
- Molécule : Assemblage électriquement neutre d’au moins deux atomes liés chimiquement (ex : molécule d’eau H₂O, molécule de dioxygène O₂).
- Ion : Atome ou groupe d’atomes ayant gagné ou perdu un ou plusieurs électrons, portant donc une charge électrique nette.
- Cation : Ion chargé positivement (a perdu des électrons, ex : ion sodium Na⁺, ion calcium Ca²⁺).
- Anion : Ion chargé négativement (a gagné des électrons, ex : ion chlorure Cl⁻, ion oxyde O²⁻).
On parle d’espèces moléculaires (constituées de molécules) et d’espèces ioniques (constituées d’ions).
L’espèce chimique « eau » est constituée d’entités « molécules H₂O ».
L’espèce chimique « chlorure de sodium » (sel de table) est constituée d’entités « ions sodium Na⁺ » et « ions chlorure Cl⁻ ». C’est un composé ionique.
Identifier l’entité : H₂SO₄ \(\rightarrow\) molécule ; Fe³⁺ \(\rightarrow\) cation ; O²⁻ \(\rightarrow\) anion ; Ar \(\rightarrow\) atome.
2. Électroneutralité de la Matière
À l’échelle macroscopique, la matière est électriquement neutre.
Dans un composé ionique (solide ou solution), les charges positives des cations compensent exactement les charges négatives des anions. Cela permet de déterminer la formule du composé.
Le chlorure de magnésium est formé d’ions magnésium Mg²⁺ et d’ions chlorure Cl⁻.
Pour assurer la neutralité, il faut deux ions Cl⁻ (charge totale 2-) pour compenser un ion Mg²⁺ (charge 2+).
La formule du composé ionique est MgCl₂.
L’oxyde d’aluminium est formé d’ions Al³⁺ et O²⁻.
Il faut 2 ions Al³⁺ (charge totale 6+) et 3 ions O²⁻ (charge totale 6-) pour la neutralité.
La formule est Al₂O₃.
Partie 2 : L’Atome et son Noyau
1. Structure de l’Atome
Un atome est constitué :
- D’un noyau central, très petit et dense, chargé positivement, qui contient des protons (charge +e) et des neutrons (charge 0). Le noyau concentre la quasi-totalité de la masse de l’atome.
- D’un cortège électronique (ou nuage électronique) constitué d’électrons (charge -e) qui gravitent autour du noyau.
Un atome est électriquement neutre : il contient autant d’électrons que de protons.
Ordre de grandeur : Le rayon de l’atome est d’environ \(10^{-10}\) m (0,1 nanomètre), tandis que celui du noyau est environ 100 000 fois plus petit (\(10^{-15}\) m). L’atome est donc essentiellement constitué de vide (« structure lacunaire »).
2. Composition du Noyau et Notation \(^A_Z X\)
Le noyau d’un atome X est caractérisé par :
- Le numéro atomique \(Z\) : Nombre de protons. C’est ce nombre qui définit l’élément chimique (tous les atomes ayant le même Z appartiennent au même élément). \(Z\) est aussi égal au nombre d’électrons dans l’atome neutre.
- Le nombre de masse \(A\) : Nombre total de nucléons (protons + neutrons).
- Le nombre de neutrons \(N\) est donc \(N = A – Z\).
Notation conventionnelle : On représente un noyau (ou l’atome) par le symbole \(^A_Z X\).
L’atome de carbone 12 : \(^{12}_6 C\).
\(Z=6 \Rightarrow\) 6 protons (c’est l’élément Carbone), et 6 électrons.
\(A=12 \Rightarrow\) 12 nucléons au total.
Nombre de neutrons \(N = A – Z = 12 – 6 = 6\).
Le noyau \(^{23}_{11} Na\) :
C’est l’élément Sodium (Na) car \(Z=11\) (11 protons). L’atome a 11 électrons.
Il a \(A=23\) nucléons.
Nombre de neutrons \(N = 23 – 11 = 12\).
3. Masse et Charge des Particules
Masses approchées :
- \(m_{\text{proton}} \approx m_{\text{neutron}} \approx 1,67 \times 10^{-27}\) kg.
- \(m_{\text{électron}} \approx 9,11 \times 10^{-31}\) kg (environ 1800 fois plus léger qu’un nucléon).
Charges électriques :
- Charge élémentaire : \(e \approx 1,60 \times 10^{-19}\) C (Coulomb).
- Charge du proton : \(+e\).
- Charge du neutron : 0.
- Charge de l’électron : \(-e\).
La masse approchée d’un atome \(^A_Z X\) est \(m_{\text{atome}} \approx A \times m_{\text{nucléon}}\) (la masse des électrons est négligeable).
Partie 3 : Le Cortège Électronique et Propriétés Chimiques
La répartition des électrons autour du noyau détermine comment l’atome va réagir chimiquement.
1. Configuration Électronique (Z ≤ 18)
Les électrons se répartissent dans des couches (numérotées 1, 2, 3…) et des sous-couches (s, p…). On remplit les sous-couches par ordre d’énergie croissante : 1s, 2s, 2p, 3s, 3p…
Capacité maximale des sous-couches :
- Sous-couche s : 2 électrons.
- Sous-couche p : 6 électrons.
La configuration électronique à l’état fondamental décrit cette répartition. On écrit le nom de la sous-couche avec le nombre d’électrons en exposant.
Oxygène (O) : \(Z=8\). 8 électrons à placer.
1s : 2 électrons (\(1s^2\)). Reste 6.
2s : 2 électrons (\(2s^2\)). Reste 4.
2p : 4 électrons (\(2p^4\)). Reste 0.
Configuration : \(1s^2 2s^2 2p^4\).
Sodium (Na) : \(Z=11\). 11 électrons.
1s², 2s², 2p⁶ (total 10 e⁻). Reste 1.
3s : 1 électron (\(3s^1\)).
Configuration : \(1s^2 2s^2 2p^6 3s^1\).
2. Électrons de Valence
Les électrons de valence sont les électrons de la dernière couche électronique occupée. Ce sont eux qui interviennent dans les liaisons chimiques.
Oxygène (O) : \(1s^2 \underline{2s^2 2p^4}\). Dernière couche n=2. Il y a \(2+4=6\) électrons de valence.
Sodium (Na) : \(1s^2 2s^2 2p^6 \underline{3s^1}\). Dernière couche n=3. Il y a 1 électron de valence.
Chlore (Cl) : \(Z=17\). \(1s^2 2s^2 2p^6 \underline{3s^2 3p^5}\). Dernière couche n=3. Il y a \(2+5=7\) électrons de valence.
3. Lien avec le Tableau Périodique (Blocs s et p)
La configuration électronique détermine la position de l’élément dans le tableau périodique (pour Z ≤ 18) :
- Le numéro de la dernière couche occupée (\(n\)) donne le numéro de la période (ligne).
- Le nombre d’électrons de valence donne (grossièrement) le numéro de la colonne (groupe). Plus précisément :
- Si la dernière sous-couche remplie est ‘s’ (\(ns^1\) ou \(ns^2\)), l’élément est dans le bloc s (colonnes 1 ou 2).
- Si la dernière sous-couche remplie est ‘p’ (\(ns^2 np^1\) à \(ns^2 np^6\)), l’élément est dans le bloc p (colonnes 13 à 18). Le numéro de colonne est \(10 + \text{nb e⁻ de valence}\).
Les éléments d’une même colonne (famille chimique) ont le même nombre d’électrons de valence et ont donc des propriétés chimiques similaires.
Sodium (Na) : \(…3s^1\). Dernière couche n=3 \(\rightarrow\) Période 3. Bloc s, 1 e⁻ de valence \(\rightarrow\) Colonne 1 (Alcalins).
Chlore (Cl) : \(…3s^2 3p^5\). Dernière couche n=3 \(\rightarrow\) Période 3. Bloc p, 7 e⁻ de valence \(\rightarrow\) Colonne 17 (Halogènes).
Argon (Ar) : \(Z=18\). \(…3s^2 3p^6\). Dernière couche n=3 \(\rightarrow\) Période 3. Bloc p, 8 e⁻ de valence \(\rightarrow\) Colonne 18 (Gaz nobles).
4. Famille des Gaz Nobles
Les gaz nobles (colonne 18 : He, Ne, Ar…) ont leur dernière couche électronique pleine (2 électrons pour He, 8 pour les autres).
Cette configuration est particulièrement stable, ce qui explique leur faible réactivité chimique.
Les autres atomes cherchent à atteindre cette stabilité en formant des ions (gagner/perdre des électrons) ou des molécules (partager des électrons) pour avoir la même configuration électronique que le gaz noble le plus proche (Règle du duet/octet).
Sodium (Na, \(…3s^1\)) perd facilement 1 e⁻ pour devenir Na⁺ (\(…2s^2 2p^6\), comme le Néon).
Chlore (Cl, \(…3s^2 3p^5\)) gagne facilement 1 e⁻ pour devenir Cl⁻ (\(…3s^2 3p^6\), comme l’Argon).
Partie 4 : Entraînement (Exercices)
-
Exercice 1 (Notation Noyau) : Un atome de phosphore (P) a 15 protons et 16 neutrons.
a) Quel est son numéro atomique Z ? Son nombre de masse A ?
b) Donner son écriture conventionnelle \(^A_Z X\).
c) Combien d’électrons possède l’atome de phosphore ? -
Exercice 2 (Configuration Électronique) : Donner la configuration électronique à l’état fondamental des atomes suivants et indiquer leur nombre d’électrons de valence :
a) Béryllium (Be, Z=4)
b) Soufre (S, Z=16) -
Exercice 3 (Tableau Périodique) : Un élément a pour configuration \(1s^2 2s^2 2p^3\).
a) Quel est son numéro atomique Z ? Quel est cet élément ?
b) À quelle période et quelle colonne appartient-il ?
c) À quelle famille chimique connue pourrait-il appartenir (donner un exemple d’élément de cette famille) ? - Exercice 4 (Composés Ioniques) : Quels ions forment le potassium (K, Z=19) et le soufre (S, Z=16) pour ressembler au gaz noble le plus proche ? En déduire la formule du sulfure de potassium.
Partie 5 : Corrections Détaillées
Correction Exercice 1 (Notation Noyau)
a) Z et A :
Nombre de protons = Numéro atomique \(Z = 15\).
Nombre de nucléons = Protons + Neutrons = \(A = 15 + 16 = 31\).
b) Écriture conventionnelle : \(^{31}_{15} P\).
c) Nombre d’électrons : Dans un atome neutre, Nombre d’électrons = Nombre de protons = Z.
Il y a 15 électrons.
Correction Exercice 2 (Configuration Électronique)
a) Béryllium (Be, Z=4) : 4 électrons.
\(1s^2\) (2 e⁻). Reste 2.
\(2s^2\) (2 e⁻). Reste 0.
Configuration : \(1s^2 2s^2\).
Dernière couche n=2. Électrons de valence : 2.
b) Soufre (S, Z=16) : 16 électrons.
\(1s^2\) (2 e⁻). Reste 14.
\(2s^2\) (2 e⁻). Reste 12.
\(2p^6\) (6 e⁻). Reste 6.
\(3s^2\) (2 e⁻). Reste 4.
\(3p^4\) (4 e⁻). Reste 0.
Configuration : \(1s^2 2s^2 2p^6 3s^2 3p^4\).
Dernière couche n=3. Électrons de valence : \(2+4 = \) 6.
Correction Exercice 3 (Tableau Périodique)
Configuration : \(1s^2 2s^2 2p^3\).
a) Identification : Nombre total d’électrons = \(2+2+3 = 7\).
Dans un atome neutre, Z = Nombre d’électrons. Donc \(Z=7\).
L’élément est l’Azote (N).
b) Position :
Dernière couche occupée : n=2 \(\rightarrow\) Période 2.
Nombre d’électrons de valence (couche n=2) : \(2+3=5\). C’est le bloc p.
Colonne = \(10 + 5 = 15\). \(\rightarrow\) Colonne 15.
c) Famille : La colonne 15 est la famille des Pnictogènes. L’élément le plus connu après l’azote est le Phosphore (P).
Correction Exercice 4 (Composés Ioniques)
Potassium (K, Z=19) : Config = \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\). Gaz noble le plus proche = Argon (Ar, Z=18, \(…3p^6\)).
Pour ressembler à l’Argon, le Potassium doit perdre son électron \(4s^1\).
Il forme l’ion K⁺.
Soufre (S, Z=16) : Config = \(1s^2 2s^2 2p^6 3s^2 3p^4\). Gaz noble le plus proche = Argon (Ar, Z=18, \(…3p^6\)).
Pour ressembler à l’Argon, le Soufre doit gagner 2 électrons pour remplir sa couche 3p.
Il forme l’ion S²⁻.
Formule du Sulfure de Potassium :
Il faut assurer la neutralité électrique. On a des ions K⁺ et S²⁻.
Il faut deux ions K⁺ (charge totale 2+) pour compenser un ion S²⁻ (charge 2-).
La formule est K₂S.
Besoin d'aide en Physique-chimie ?
Je propose des cours de remise à niveau en visio ou en présentiel