FICHE DE RÉVISION – Détermination d'une Quantité de Matière : Le Titrage
(Niveau : Première)
Détermination d’une Quantité de Matière : Le Titrage
Utiliser une réaction chimique maîtrisée (le titrage) pour trouver une concentration inconnue.
Partie 1 : Qu’est-ce qu’un Titrage ?
Un titrage (ou dosage) est une technique expérimentale qui permet de déterminer la concentration inconnue d’une espèce chimique (le « titré ») en la faisant réagir avec une autre espèce de concentration connue (le « titrant »).
Pour être utilisée pour un titrage, la réaction chimique doit être :
- Rapide : L’effet doit être instantané.
- Totale : La réaction doit être complète (le réactif limitant disparaît totalement).
- Unique : Il ne doit pas y avoir d’autres réactions parasites.
Nous étudions ici le **titrage avec suivi colorimétrique**, où l’on repère la fin du titrage grâce à un changement de couleur.
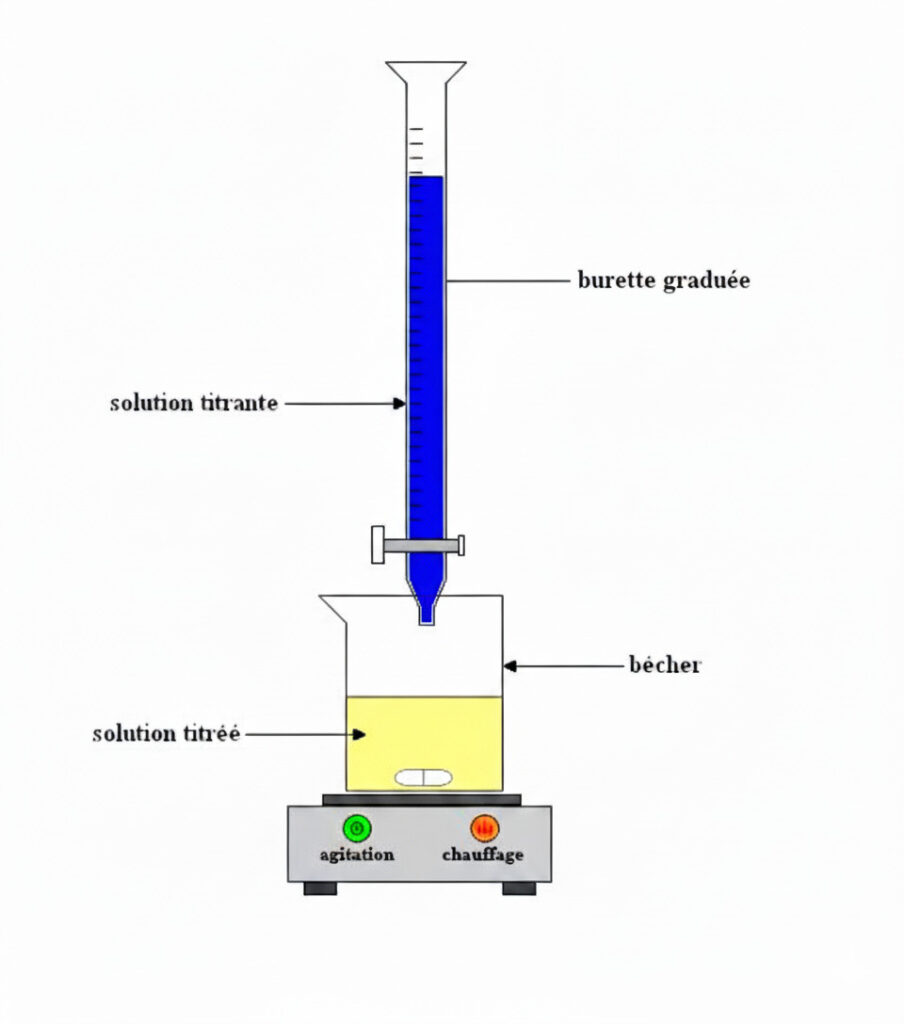
Partie 2: Montage et Vocabulaire 💧
Le montage d’un titrage est très standardisé.
Vocabulaire :
- La Burette Graduée : Contient la solution titrante (de concentration CA connue). Elle permet de mesurer très précisément le volume versé (VA).
- Le Bécher (ou Erlenmeyer) : Contient la solution titrée (de concentration CB inconnue, mais de volume VB connu et précis).
- L’Agitateur Magnétique : Permet de mélanger la solution instantanément pour que la réaction soit homogène.
Partie 3 : L’Équivalence (Le Moment Clé)
L’équivalence est le moment précis du titrage où l’on a versé juste assez de réactif A (titrant) pour consommer tout le réactif B (titré).
Définition : À l’équivalence, les réactifs (titrant A et titré B) ont été introduits dans les proportions stœchiométriques de l’équation bilan.
À ce point, les deux réactifs sont limitants et ont été totalement consommés.
- Avant l’équivalence : On verse le titrant A. Il est immédiatement consommé. Le titré B est en excès.
(Réactif limitant = Titrant A) - Après l’équivalence : On a épuisé tout le titré B. Le titrant A qu’on continue de verser ne réagit plus et s’accumule.
(Réactif limitant = Titré B)
Partie 4 : Repérage de l’Équivalence (Colorimétrie)
Comment « voir » ce moment précis ? On se fie à un changement de couleur brutal.
Cas 1 : L’un des réactifs (ou produits) est très coloré.
C’est le cas le plus simple. On utilise souvent l’ion permanganate (MnO4–), qui est violet intense.
Exemple : On titre des ions Fe2+ (incolores) par du MnO4– (violet).
– Avant l’équivalence : Le MnO4– qu’on verse est limitant, il réagit et se transforme en Mn2+ (incolore). Le bécher reste incolore.
– À l’équivalence (la goutte près) : Tout le Fe2+ est consommé. La goutte de MnO4– suivante qu’on verse ne peut plus réagir, elle reste.
– Résultat : Le bécher passe de l’incolore au violet/rose persistant. C’est l’équivalence !
Cas 2 : Tous les réactifs sont incolores.
On ajoute un indicateur coloré. C’est une espèce chimique qu’on ajoute en très faible quantité et qui change de couleur pile au moment de l’équivalence.
Partie 5 : La Relation à l’Équivalence 📊
C’est le but du titrage : trouver la relation mathématique qui permet de calculer la concentration inconnue CB.
Soit la réaction de titrage : a A + b B → c C + d D
(Avec A = titrant et B = titré)
À l’équivalence, les réactifs ont été introduits en proportions stœchiométriques. Cela s’écrit :
nA, versé / a = nB, initial / b
On remplace les quantités de matière par les concentrations et volumes :
nA, versé = CA x VAE
nB, initial = CB x VB
On obtient la relation d’équivalence :
(CA x VAE) / a = (CB x VB) / b
- CA : Concentration du titrant (connue, en mol/L)
- VAE : Volume à l’équivalence (lu sur la burette, en L ou mL)
- CB : Concentration du titré (l’inconnue, en mol/L)
- VB : Volume initial du titré (connu, en L ou mL)
- a, b : Coefficients stœchiométriques de la réaction
Le plus often, on cherche CB :
CB = (CA x VAE x b) / (a x VB)
(Note : Si VAE et VB sont tous les deux en mL, ça marche, les unités s’annulent).
Partie 6 : Entraînement (Exercices)
-
Exercice 1 (Vocabulaire) : On veut trouver la concentration d’une solution d’eau oxygénée (H2O2) dans un bécher. On utilise une solution de permanganate de potassium (KMnO4) de concentration 0,1 mol/L dans la burette.
Identifier le réactif titrant et le réactif titré. -
Exercice 2 (Relation d’équivalence) : On réalise le titrage de VB = 20,0 mL d’une solution d’ions Fer II (Fe2+) par une solution de permanganate (MnO4–) de concentration CA = 0,02 mol/L.
L’équation de la réaction (simplifiée) est :
1 MnO4– + 5 Fe2+ → …
On repère l’équivalence lorsque VAE = 12,0 mL.
a) Écrire la relation d’équivalence.
b) Calculer la concentration CB des ions Fe2+.
Partie 7 : Corrections Détaillées
Correction Exercice 1 (Vocabulaire)
Réactif titrant : C’est la solution de concentration connue, dans la burette.
→ Le permanganate de potassium (KMnO4).
Réactif titré : C’est la solution de concentration inconnue, dans le bécher.
→ L’eau oxygénée (H2O2).
Correction Exercice 2 (Relation d’équivalence)
Données :
A = MnO4– (titrant) ; B = Fe2+ (titré)
a = 1 ; b = 5
CA = 0,02 mol/L
VB = 20,0 mL
VAE = 12,0 mL
a) Relation d’équivalence :
(CA x VAE) / a = (CB x VB) / b
(CA x VAE) / 1 = (CB x VB) / 5
b) Calcul de CB :
On isole CB : CB = (5 x CA x VAE) / (1 x VB)
CB = (5 x 0,02 x 12,0) / 20,0
(On peut laisser VAE et VB en mL car le rapport s’annule)
CB = 1,2 / 20,0
CB = 0,06 mol/L
La concentration en ions Fer II est de 0,06 mol/L.
Besoin d'aide en Physique-chimie ?
Je propose des cours de remise à niveau en visio ou en présentiel

