FICHE DE RÉVISION – Structure des entités et polarité
(Niveau : Première)
Structure des Entités et Polarité
Du schéma de Lewis à la géométrie et à la polarité des molécules : comprendre les liaisons chimiques.
Partie 1 : Schéma de Lewis (Molécules et Ions)
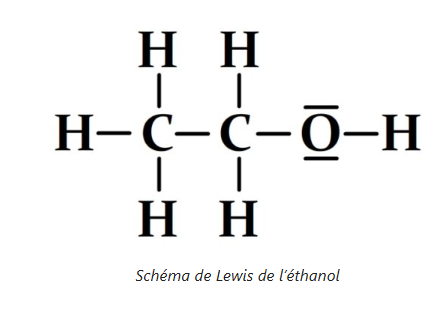
Le schéma de Lewis est une représentation plane des liaisons covalentes et des doublets non-liants d’une molécule ou d’un ion polyatomique, basée sur les électrons de valence.
1. Rappel : Électrons de Valence et Règle de Stabilité
- Les électrons de valence sont ceux de la dernière couche électronique. Leur nombre est donné (pour les blocs s et p) par le numéro de la colonne dans le tableau périodique (1 pour H, Li, Na… ; 2 pour Be, Mg… ; 13 pour B, Al… ; 14 pour C, Si… ; 15 pour N, P… ; 16 pour O, S… ; 17 pour F, Cl… ; 18 pour Ne, Ar…).
- Règle de Stabilité (Duet/Octet) : Les atomes (Z ≤ 18) tendent à s’entourer de 2 électrons (pour H, Li, Be) ou 8 électrons (pour les autres) sur leur couche de valence pour acquérir la stabilité d’un gaz noble.
- Une liaison covalente (simple, double ou triple) est formée par la mise en commun d’électrons entre deux atomes. Chaque liaison compte pour 2 électrons pour chaque atome lié.
- Un doublet non-liant est une paire d’électrons de valence appartenant à un seul atome et ne participant pas à une liaison.
2. Méthode pour Établir un Schéma de Lewis
Pour une molécule ou un ion polyatomique (pour Z ≤ 18) :
- Compter le nombre total d’électrons de valence (Nval) : Somme des électrons de valence de tous les atomes. Attention : Ajouter ou retirer des électrons si c’est un ion (ex: ajouter 1e⁻ pour OH⁻, retirer 1e⁻ pour NH₄⁺).
- Compter le nombre total de doublets (Nd) : Diviser Nval par 2 (\(N_d = N_{val} / 2\)).
- Identifier l’atome central : Souvent l’atome le moins électronégatif (sauf H) ou celui qui fait le plus de liaisons (ex: C dans CH₄, N dans NH₃).
- Placer les liaisons simples : Relier l’atome central aux autres atomes par des liaisons simples (doublets liants).
- Répartir les doublets restants : Placer les doublets non-liants restants sur les atomes périphériques (sauf H) pour satisfaire leur règle de l’octet, puis sur l’atome central si nécessaire.
- Vérifier l’octet (ou duet) : Si un atome (souvent le central) n’a pas son octet, transformer des doublets non-liants d’atomes voisins en doublets liants (liaisons multiples : double =, triple ≡) jusqu’à ce que tous les atomes (sauf H) respectent l’octet.
- Indiquer la charge (pour les ions) : Mettre le schéma entre crochets et indiquer la charge globale en exposant.
Molécule d’ammoniac NH₃ :
1. N (col 15 -> 5 e⁻ val.), H (col 1 -> 1 e⁻ val.). \(N_{val} = 5 + 3 \times 1 = 8\) e⁻.
2. \(N_d = 8 / 2 = 4\) doublets à placer.
3. Atome central : N.
4. Liaisons simples : N–H (3 fois). 3 doublets liants utilisés.
5. Doublets restants : 4 – 3 = 1 doublet non-liant. On le place sur N (H ne peut pas en avoir).
Schéma : H–N̈–H (avec un H en dessous ou au-dessus).
6. Vérification : Chaque H a 1 doublet liant (duet OK). N a 3 liants + 1 non-liant = 4 doublets (octet OK).
Le schéma de Lewis est correct.
Ion Hydroxide OH⁻ :
1. O (6 e⁻ val.), H (1 e⁻ val.), Charge – (1 e⁻ en plus). \(N_{val} = 6 + 1 + 1 = 8\) e⁻.
2. \(N_d = 8 / 2 = 4\) doublets.
3. Pas vraiment d’atome central.
4. Liaison simple O–H. 1 doublet utilisé.
5. Doublets restants : 4 – 1 = 3 doublets non-liants. On les place sur O (H ne peut pas).
Schéma : [ :Ö–H ]⁻ (3 doublets non-liants sur O).
6. Vérification : H a 1 liant (duet OK). O a 1 liant + 3 non-liants = 4 doublets (octet OK).
7. Indiquer la charge : [ :Ö–H ]⁻. Correct.
3. Lacune Électronique
Une lacune électronique existe sur un atome dans un schéma de Lewis si cet atome est entouré de moins de 4 doublets (moins de 8 électrons) alors qu’il pourrait en avoir 8 (typiquement Bore B, Aluminium Al…). L’entité est souvent très réactive.
Trifluorure de Bore BF₃ : B (3 e⁻ val.), F (7 e⁻ val.). \(N_{val} = 3 + 3 \times 7 = 24\) e⁻. \(N_d = 12\).
Schéma : B central, 3 liaisons B–F. 3 doublets liants utilisés. Reste 9.
On place 3 doublets non-liants sur chaque F (pour leur octet). 3×3=9 doublets utilisés.
Vérification : Chaque F a 1 liant + 3 non-liants = 4 doublets (OK). Mais B n’a que 3 liaisons = 3 doublets. Il a une lacune électronique.
Partie 2 : Géométrie des Entités
Le schéma de Lewis permet de prévoir la forme tridimensionnelle d’une molécule ou d’un ion (Méthode VSEPR simplifiée).
Principe : Les doublets électroniques (liants et non-liants) autour de l’atome central se repoussent électriquement et s’écartent au maximum les uns des autres.
Formes typiques autour d’un atome central A (pour Z ≤ 18) :
- 2 liaisons, 0 non-liant (AX₂) : Linéaire (ex: CO₂). Angle ≈ 180°.
- 3 liaisons, 0 non-liant (AX₃) : Triangulaire plane (ex: BF₃). Angles ≈ 120°.
- 4 liaisons, 0 non-liant (AX₄) : Tétraédrique (ex: CH₄). Angles ≈ 109.5°.
- 3 liaisons, 1 non-liant (AX₃E) : Pyramidale à base triangulaire (ex: NH₃). Angles < 109.5° (≈ 107°).
- 2 liaisons, 2 non-liants (AX₂E₂) : Coudée (ou forme en V) (ex: H₂O). Angle < 109.5° (≈ 104.5°).
(E représente un doublet non-liant. Les liaisons multiples comptent comme une seule direction pour la géométrie).
NH₃ : 3 liaisons, 1 non-liant sur N (AX₃E) \(\rightarrow\) Géométrie pyramidale.
H₂O : 2 liaisons, 2 non-liants sur O (AX₂E₂) \(\rightarrow\) Géométrie coudée.
CH₄ : 4 liaisons, 0 non-liant sur C (AX₄) \(\rightarrow\) Géométrie tétraédrique.
Partie 3 : Électronégativité et Polarité
1. Électronégativité
L’électronégativité d’un atome mesure sa capacité à attirer vers lui les électrons d’une liaison covalente dans laquelle il est engagé.
Elle est donnée par une valeur numérique (échelle de Pauling la plus courante).
Évolution dans le tableau périodique (simplifiée) : L’électronégativité augmente globalement de gauche à droite sur une période et de bas en haut dans une colonne.
(Fluor F est le plus électronégatif, Oxygène O et Azote N sont très électronégatifs, Hydrogène H et Carbone C sont moyennement électronégatifs, métaux alcalins Na, K sont peu électronégatifs).
2. Polarisation d’une Liaison
Une liaison covalente entre deux atomes A et B est polarisée si les atomes A et B ont des électronégativités différentes.
L’atome le plus électronégatif attire davantage les électrons du doublet liant. Il porte alors une charge partielle négative \(\delta-\), tandis que l’autre atome porte une charge partielle positive \(\delta+\).
La liaison est d’autant plus polarisée que la différence d’électronégativité est grande.
Si la différence est nulle (liaison entre atomes identiques, ex: H–H, O=O) ou très faible (ex: C–H), la liaison est considérée comme apolaire (ou très peu polaire).
Liaison O–H (dans H₂O) : O est beaucoup plus électronégatif que H. La liaison est fortement polarisée : \(^{\delta+}H – O^{\delta-}\).
Liaison C–H (dans CH₄) : C et H ont des électronégativités proches. La liaison est considérée apolaire.
Liaison C=O (dans CO₂) : O est plus électronégatif que C. La liaison est polarisée : \(^{\delta+}C = O^{\delta-}\).
3. Polarité d’une Molécule
Une molécule est polaire si le « barycentre » (centre géométrique) des charges partielles positives \(\delta+\) ne coïncide pas avec celui des charges partielles négatives \(\delta-\).
Une molécule est apolaire si ces barycentres coïncident.
Conditions pour être polaire :
- La molécule doit contenir au moins une liaison polarisée.
- La géométrie de la molécule doit être telle que les polarités des liaisons ne s’annulent pas mutuellement.
En général, une molécule avec des liaisons polarisées est apolaire si sa géométrie est très symétrique (ex: linéaire AX₂, triangulaire plane AX₃, tétraédrique AX₄) ET que tous les atomes liés à l’atome central sont identiques.
Eau H₂O : Liaisons O–H polarisées. Géométrie coudée (non symétrique). Les polarités ne s’annulent pas. L’eau est une molécule très polaire.
Dioxyde de carbone CO₂ : Liaisons C=O polarisées. Géométrie linéaire O=C=O (symétrique). Les deux polarités C\(\to\)O s’annulent. CO₂ est une molécule apolaire.
Méthane CH₄ : Liaisons C–H (quasi) apolaires. Géométrie tétraédrique (symétrique). CH₄ est une molécule apolaire.
Ammoniac NH₃ : Liaisons N–H polarisées (N plus électronégatif). Géométrie pyramidale (non symétrique à cause du doublet non-liant). NH₃ est une molécule polaire.
1. Regarde si les liaisons sont polarisées (atomes différents et électronégativités différentes). Si non \(\rightarrow\) apolaire.
2. Si oui, regarde la géométrie autour de l’atome central. Si c’est parfaitement symétrique (linéaire, triangulaire, tétraédrique) ET que tous les « bras » sont identiques \(\rightarrow\) apolaire. Sinon (coudée, pyramidale, ou « bras » différents) \(\rightarrow\) polaire.
Partie 4 : Entraînement (Exercices)
-
Exercice 1 (Schéma de Lewis) : Établir le schéma de Lewis des entités suivantes :
a) Molécule de Chlorure d’hydrogène HCl (Cl: Z=17)
b) Ion Ammonium NH₄⁺ (N: Z=7, H: Z=1) -
Exercice 2 (Géométrie) : Prédire la géométrie des molécules suivantes à partir de leur schéma de Lewis (que l’on admettra ou que l’on construira) :
a) Dichlorométhane CH₂Cl₂ (C central, lié à 2 H et 2 Cl)
b) Dioxyde de soufre SO₂ (S central, lié à 2 O par des doubles liaisons, 1 doublet non-liant sur S) -
Exercice 3 (Polarité) : Les molécules suivantes sont-elles polaires ou apolaires ? Justifier. (Électronégativités : F > O > Cl > N > C > H)
a) Difluor F₂
b) Chlorure d’hydrogène HCl
c) Tétrachlorométhane CCl₄ (géométrie tétraédrique)
Partie 5 : Corrections Détaillées
Correction Exercice 1 (Schéma de Lewis)
a) HCl : H (1 e⁻ val.), Cl (col 17 -> 7 e⁻ val.). \(N_{val} = 1 + 7 = 8\) e⁻. \(N_d = 4\) doublets.
– Liaison simple H–Cl (1 doublet). Reste 3.
– Placer les 3 non-liants sur Cl (pour son octet). H n’en prend pas.
– Schéma : H–Cl: (avec 3 doublets non-liants sur Cl).
– Vérification : H a 1 liant (duet OK). Cl a 1 liant + 3 non-liants = 4 doublets (octet OK).
Solution : H–:C̈l: (Les points représentent les électrons des doublets non-liants).
b) Ion Ammonium NH₄⁺ : N (5 e⁻ val.), H (1 e⁻ val. \(\times\) 4), Charge + (1 e⁻ en moins).
\(N_{val} = 5 + 4 \times 1 – 1 = 8\) e⁻. \(N_d = 4\) doublets.
– Atome central : N.
– 4 liaisons simples N–H (4 doublets). Reste 0.
– Schéma : [ N au centre, lié à 4 H ]⁺.
– Vérification : Chaque H a 1 liant (duet OK). N a 4 liants = 4 doublets (octet OK).
Solution : [ H–N(H)(H)–H ]⁺ (avec N au centre).
Correction Exercice 2 (Géométrie)
a) Dichlorométhane CH₂Cl₂ : C est l’atome central. Il est lié à 4 autres atomes (2 H, 2 Cl) et n’a pas de doublet non-liant (C a 4 e⁻ val., il fait 4 liaisons).
C’est une structure de type AX₄.
Géométrie : Tétraédrique (autour du Carbone).
b) Dioxyde de soufre SO₂ : S est l’atome central. Il est lié à 2 atomes O et possède 1 doublet non-liant.
C’est une structure de type AX₂E (les doubles liaisons comptent comme une seule direction).
Géométrie : Coudée (ou forme en V) autour du Soufre.
Correction Exercice 3 (Polarité)
a) Difluor F₂ : Molécule F–F.
La liaison est entre deux atomes identiques, donc apolaire.
La molécule F₂ est apolaire.
b) Chlorure d’hydrogène HCl : Molécule H–Cl.
Cl est plus électronégatif que H. La liaison H–Cl est polarisée (\(^{\delta+}H – Cl^{\delta-}\)).
Comme il n’y a qu’une seule liaison, la molécule est forcément polaire.
c) Tétrachlorométhane CCl₄ : Molécule avec C central lié à 4 Cl. Géométrie tétraédrique.
Cl est plus électronégatif que C. Les liaisons C–Cl sont polarisées (\(^{\delta+}C – Cl^{\delta-}\)).
MAIS la géométrie est tétraédrique, qui est très symétrique. Les 4 vecteurs polarité des liaisons C–Cl se compensent exactement (leur somme vectorielle est nulle).
La molécule CCl₄ est apolaire.
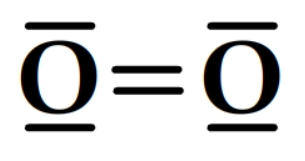
Besoin d'aide en Physique-chimie ?
Je propose des cours de remise à niveau en visio ou en présentiel

